წარმოიდგინეთ მომავალი, სადაც კიბოსა და რთული აუტოიმუნური დაავადებების მკურნალობა ისეთივე მარტივია, როგორც ერთი ინექციის გაკეთება. მომავალი, სადაც პაციენტის საკუთარი უჯრედები, ლაბორატორიის კედლების მიღმა, პირდაპირ ორგანიზმშივე იქცევიან კიბოს უჯრედებზე მომართულ “სუპერ-ჯარისკაცებად“.
ეს ფანტასტიკის სფეროს აღარ განეკუთვნება. ეს რეალობა ერთი ნაბიჯით მოგვიახლოვდა მას შემდეგ, რაც პენსილვანიის უნივერსიტეტის მეცნიერებმა, ბიოტექნოლოგიურ კომპანია Capstan Therapeutics-თან თანამშრომლობით, თავიანთი კვლევის შედეგები მსოფლიოს ერთ-ერთ ყველაზე პრესტიჟულ სამეცნიერო ჟურნალში – Science – გამოაქვეყნეს.
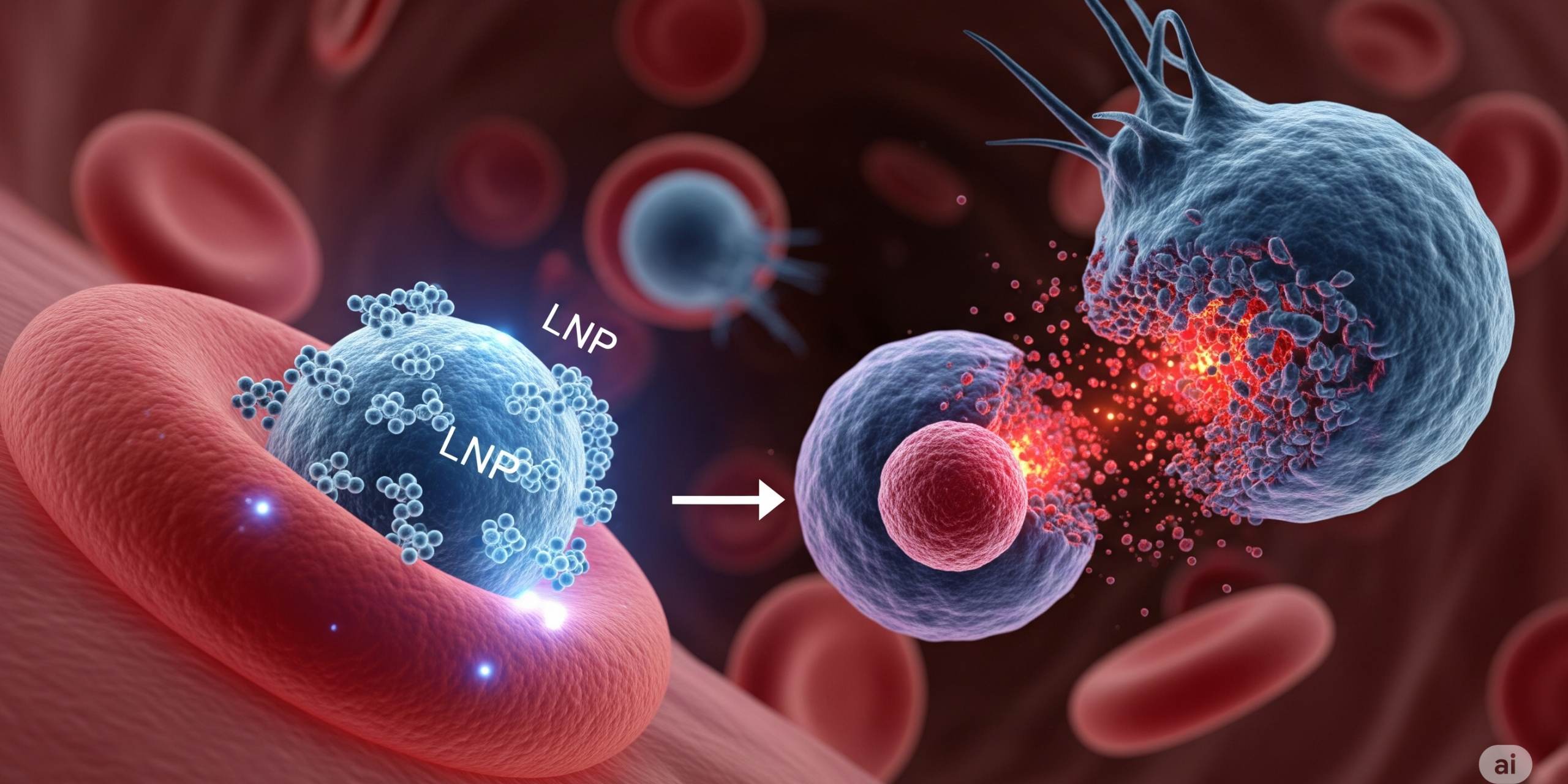
კვლევა დეტალურად აღწერს, თუ როგორ შეიძლება ერთი ინექციით, mRNA ტექნოლოგიისა და ლიპიდური ნანონაწილაკების (LNP) მეშვეობით, პაციენტის იმუნური T-უჯრედები პირდაპირ ორგანიზმშივე გადაიქცნენ მძლავრ CAR-T უჯრედებად. ეს აღმოჩენა საფუძველს უყრის კიბოსა და აუტოიმუნური დაავადებების მკურნალობის სრულიად ახალ, „მზა“ (off-the-shelf) მიდგომას.
კვლევის მიზანი: როგორ დავძლიოთ არსებული თერაპიის ბარიერები?
სანამ ახალ აღმოჩენას ჩავუღრმავდებით, გავიგოთ, რა პრობლემის გადაჭრას ცდილობდნენ მეცნიერები. თანამედროვე იმუნოთერაპიას უკვე აქვს მძლავრი იარაღი – CAR-T თერაპია, რომელმაც სისხლის კიბოს ზოგიერთი სახეობის მკურნალობაში რევოლუცია უკვე მოახდინა. თუმცა, მას აქვს სამი დიდი მინუსი:
- სირთულე და დრო: პაციენტის იმუნური უჯრედების ამოღება, ლაბორატორიაში მათი გენეტიკური შეცვლა და ორგანიზმში დაბრუნება კვირებს მოითხოვს.
- ღირებულება: პროცესი ასობით ათასი დოლარი ჯდება, რაც მას ბევრი პაციენტისთვის მიუწვდომელს ხდის.
- მძიმე გვერდითი ეფექტები: თერაპიას ხშირად თან ახლავს მძიმე, ზოგჯერ სიცოცხლისთვის საშიში გართულებები.
კვლევის მთავარი მიზანი იყო ამ ბარიერების დანგრევა – შეექმნათ CAR-T უჯრედების მიღების ისეთი მეთოდი, რომელიც იქნებოდა სწრაფი, იაფი, უსაფრთხო და ყველასთვის ხელმისაწვდომი.
ოთხი არმია კიბოს წინააღმდეგ: დეტალური გზამკვლევი იმუნოთერაპიაში
ბოლო პერიოდში ხშირად ვწერთ კიბოსთან ბრძოლის აღალ-ახალი მეთოდების შესახებ. ალბათ გახსოვთ სტატიაც “5-წუთიანი იმუნოთერაპია 15 ტიპის კიბოს წინააღმდეგ”
იმისათვის, რომ სრულად გავიგოთ, სად დგას ახალი აღმოჩენა, მოდით, დაწვრილებით შევისწავლოთ კიბოსთან მებრძოლი ოთხივე “არმიის“ სტრატეგია, მათი ძლიერი და სუსტი მხარეები.
1. ტრადიციული CAR-T თერაპია: “ლაბორატორიაში შექმნილი არმია“
-
რა არის ეს? ეს არის პერსონალიზებული უჯრედული თერაპია, ანუ „ცოცხალი წამალი“, რომელიც პაციენტის საკუთარი უჯრედებისგან იქმნება. ის დღესდღეობით ერთ-ერთი ყველაზე მძლავრი იმუნოთერაპიული იარაღია სისხლის კიბოს გარკვეული სახეობების წინააღმდეგ.
-
როგორ მუშაობს? (ეტაპობრივად)
- ჯარისკაცების შეგროვება: პაციენტს ვენიდან უღებენ სისხლს და სპეციალური აპარატით გამოყოფენ მის იმუნურ T-უჯრედებს.
- სპეც-მომზადება ლაბორატორიაში: ამ უჯრედებს გენეტიკური ინჟინერიის მეთოდით “აიარაღებენ“ — უმატებენ ქიმერული ანტიგენის რეცეპტორს (CAR). ეს რეცეპტორი არის „ჭკვიანი თვალი“, რომელიც კიბოს უჯრედის ზედაპირზე არსებულ კონკრეტულ ნიშანს (ანტიგენს) პოულობს და მასზე “იკეტება“.
- არმიის გამრავლება: მოდიფიცირებულ უჯრედებს ლაბორატორიაში ასობით მილიონამდე ამრავლებენ.
- ბრძოლის ველზე დაბრუნება: გამრავლებულ CAR-T უჯრედებს პაციენტს გადასხმის გზით უკან, ორგანიზმში უბრუნებენ, სადაც ისინი აქტიურად იწყებენ კიბოზე ნადირობას.
-
ძლიერი მხარეები: უაღრესად მაღალი ეფექტიანობა ზოგიერთი ლეიკემიისა და ლიმფომის დროს, ხშირად პაციენტებში, რომლებსაც სხვა ვერანაირი მკურნალობა ვეღარ შველით.
-
სუსტი მხარეები: პროცესი კვირებს გრძელდება, ძალიან ძვირია (ასობით ათასი დოლარი), შეიძლება გამოიწვიოს მძიმე გვერდითი ეფექტები (ციტოკინური შტორმი) და ნაკლებად ეფექტურია სოლიდური (მყარი) სიმსივნეების წინააღმდეგ.
2. თერაპიული კიბოს ვაქცინები: “არსებული არმიის გაწვრთნა“
-
რა არის ეს? ეს არის არა უჯრედული, არამედ იმუნური სისტემის მასტიმულირებელი თერაპია. მისი მიზანია, პაციენტის საკუთარ იმუნურ სისტემას „ასწავლოს“ კიბოს უჯრედების დამოუკიდებლად ამოცნობა და განადგურება.
-
როგორ მუშაობს? ვაქცინა ორგანიზმს აწვდის კიბოს უჯრედისთვის დამახასიათებელ ერთ ან რამდენიმე ანტიგენს (მაგალითად, ცილის ფრაგმენტს ან mRNA მოლეკულას, რომელიც ამ ცილის “რეცეპტს“ შეიცავს). იმუნური სისტემის “საგუშაგო“ უჯრედები ამ ანტიგენს აღიქვამენ, როგორც უცხოს და განგაშის სიგნალს აძლევენ მთელ სისტემას, მათ შორის T-უჯრედებს, რომლებიც იწყებენ ამ ანტიგენის მატარებელი ყველა უჯრედის (ანუ კიბოს უჯრედების) ძებნასა და განადგურებას. ეს ჰგავს “დამნაშავის ფოტოს“ გავრცელებას, რათა ყველა პოლიციელმა იცოდეს, ვინ უნდა დაიჭიროს.
-
ძლიერი მხარეები: პოტენციურად უფრო უნივერსალური და იაფია, ვიდრე CAR-T. შეუძლია იმუნური “მეხსიერების“ ჩამოყალიბება, რაც რეციდივის რისკს ამცირებს.
-
სუსტი მხარეები: ეფექტიანობა ცვალებადია. ზოგჯერ კიბო ახერხებს იმუნური პასუხისგან თავის დაღწევას, მიუხედავად “ტრენინგისა“.
3. ახალი in vivo CAR-T თერაპია: “მწვრთნელების დესანტი ბრძოლის ველზე“
-
რა არის ეს? ეს არის რევოლუციური ჰიბრიდი, რომელიც აერთიანებს ვაქცინის ტექნოლოგიასა და CAR-T თერაპიის მიზანს. ის გვერდს უვლის ლაბორატორიულ ეტაპს და უჯრედების მოდიფიკაციას პირდაპირ სხეულში ახდენს.
-
როგორ მუშაობს? პაციენტს ინექციით უკეთდება სპეციალური ლიპიდური ნანონაწილაკები (LNP). ეს ნანონაწილაკები, როგორც მიზანმიმართული “კაფსულები“, შეიცავენ mRNA ინსტრუქციას CAR რეცეპტორის შესაქმნელად. ისინი სისხლში პოულობენ T-უჯრედებს, ერწყმიან მათ და გადასცემენ ამ ინსტრუქციას. T-უჯრედი მიღებული “რეცეპტით“ თავად იწყებს CAR რეცეპტორების წარმოქმნას და ადგილზევე იქცევა კიბოსთან მებრძოლ ელიტურ ჯარისკაცად. პროცესი სწრაფი და ეფექტურია.
-
ძლიერი მხარეები: აერთიანებს CAR-T-ს სიმძლავრეს და ვაქცინის სიმარტივეს. პოტენციურად ბევრად სწრაფი, იაფი და ხელმისაწვდომია. mRNA-ს დროებითი ეფექტი მას უფრო უსაფრთხოს ხდის აუტოიმუნური დაავადებებისთვის.
-
სუსტი მხარეები: ტექნოლოგია ჯერ კიდევ ადრეულ, ექსპერიმენტულ ფაზაშია. საჭიროა ადამიანებზე კვლევები მისი უსაფრთხოებისა და ეფექტიანობის დასადასტურებლად.
4. იმუნური გამშვები პუნქტის ინჰიბიტორები (ნივოლუმაბი): “მუხრუჭების მომხსნელი გუნდი“
-
რა არის ეს? ეს ისაა, 5 წუთიანი ინექციის სახელით რომ ვიცნობთ. ეს არის თერაპია, რომელიც არ ქმნის ახალ ჯარისკაცებს და არც წვრთნის მათ. ის ათავისუფლებს უკვე არსებულ, მაგრამ კიბოს მიერ დაბლოკილ ჯარისკაცებს.
-
როგორ მუშაობს? კიბოს უჯრედები ეშმაკურ მექანიზმს იყენებენ: ისინი T-უჯრედის ზედაპირზე არსებულ ბუნებრივ “მუხრუჭს“ (PD-1 რეცეპტორს) ააქტიურებენ, რითაც მის გათიშვასა და იმობილიზაციას იწვევენ. ნივოლუმაბის მსგავსი წამლები არის ანტისხეულები, რომლებიც ფარივით ეფარებიან ამ “მუხრუჭს“. როდესაც კიბოს უჯრედი მის დაჭერას ცდილობს, მას ეს აღარ გამოსდის. შედეგად, T-უჯრედი თავისუფლდება ამ ბლოკისგან, “იღვიძებს“ და აღიდგენს კიბოზე შეტევის უნარს.
-
ძლიერი მხარეები: ეფექტურია მრავალი ტიპის სიმსივნის წინააღმდეგ (მელანომა, ფილტვის, თირკმლის კიბო და სხვ.). წარმოადგენს “მზა“ პრეპარატს, რომელიც არ საჭიროებს ინდივიდუალურ ლაბორატორიულ დამზადებას.
-
სუსტი მხარეები: ყველა პაციენტი არ პასუხობს მკურნალობაზე. “მუხრუჭების“ მოხსნამ ზოგჯერ შეიძლება გამოიწვიოს იმუნური სისტემის გადაჭარბებული აქტივაცია და ჯანმრთელ ქსოვილებზე შეტევა (აუტოიმუნური გვერდითი ეფექტები).
in vivo CAR-T თერაპია – კვლევის ეტაპები და შედეგები: რა აჩვენა ექსპერიმენტებმა?
კვლევა პრეკლინიკურ ფაზაში, ანუ ცხოველებზე ჩატარდა და შედეგები შთამბეჭდავი იყო:
- ეტაპი I (თაგვები, ონკოლოგია): ლიმფომით დაავადებულ თაგვებს პრეპარატის ერთი ინექცია გაუკეთეს. შედეგად, მათ ორგანიზმში სწრაფად წარმოიქმნა CAR-T უჯრედები, რომლებმაც სიმსივნე სრულად გაანადგურეს და ცხოველების სიცოცხლე მნიშვნელოვნად გახანგრძლივდა.
- ეტაპი II (პრიმატები, აუტოიმუნური მოდელი): მაიმუნებზე ჩატარებულმა ცდამ აჩვენა, რომ ინექციამ ეფექტურად გაანადგურა აუტოიმუნური დაავადებების გამომწვევი B-უჯრედები. ყველაზე მნიშვნელოვანი კი ის იყო, რომ ეს მოხდა წინასწარი, მძიმე ქიმიოთერაპიის გარეშე, რაც ტრადიციული CAR-T თერაპიის აუცილებელი და ტოქსიკური ნაწილია.
მიმდინარე ეტაპი და გამოწვევები: რა გველის წინ?
ეს შედეგები უდიდესი იმედის მომცემია, თუმცა გზა კლინიკურ გამოყენებამდე ჯერ კიდევ გასავლელია.
- მიმდინარე ეტაპი: კვლევა გადავიდა ადამიანებზე კლინიკური კვლევის პირველ ფაზაში. ამ ეტაპზე მეცნიერები ამოწმებენ პრეპარატის უსაფრთხოებას ჯანმრთელ მოხალისეებზე. თავდაპირველად, კვლევები ფოკუსირებულია აუტოიმუნურ დაავადებებზე.
- მომავლის გამოწვევები:
- უსაფრთხოება ადამიანებში: იმუშავებს თუ არა მეთოდი ადამიანებში ისევე ეფექტურად და უსაფრთხოდ, როგორც ცხოველებში? ეს მთავარი კითხვაა.
- მიზნის სიზუსტე: რამდენად ზუსტად იპოვიან ნანონაწილაკები მხოლოდ T-უჯრედებს და ხომ არ ექნებათ გავლენა სხვა, ჯანმრთელ უჯრედებზე?
- ბრძოლა სოლიდურ სიმსივნეებთან: იქნება თუ არა ეს მიდგომა ეფექტური ფილტვის, სარძევე ჯირკვლისა და სხვა სოლიდური სიმსივნეების წინააღმდეგ, სადაც ტრადიციული CAR-T თერაპია ნაკლებად წარმატებულია?
- მასშტაბური წარმოება: შესაძლებელი იქნება თუ არა ამ რთული ნანონაწილაკების სტაბილური და მასობრივი წარმოება?
დასკვნა: მიუხედავად იმისა, რომ წინ ჯერ კიდევ ბევრი სამუშაოა, ეს აღმოჩენა უდიდესი ნაბიჯია პერსონალიზებული მედიცინის მომავლისკენ. ეს არის იმედი, რომ მალე მივიღებთ “მზა ფორმით” არსებულ, ხელმისაწვდომ და უსაფრთხო უჯრედულ თერაპიებს, რომლებიც შეცვლიან არა მხოლოდ კიბოს, არამედ მრავალი სხვა მძიმე დაავადების მკურნალობის პრინციპებს.