ლაიმის დაავადება უკვე ათწლეულებია ერთ-ერთ ყველაზე მნიშვნელოვან ტკიპებით გადამდებ ინფექციად ითვლება მთელს მსოფლიოში, განსაკუთრებით ჩრდილოეთ ნახევარსფეროში. ის გამოწვეულია ბორელიას გვარის ბაქტერიებით და ადამიანზე, როგორც წესი, ინფიცირებული Ixodes ტკიპის ნაკბენით გადადის. დაავადება ადრეულ ეტაპზე შეიძლება გამოვლინდეს სიცხით, დაღლილობით, თავის ტკივილით და დამახასიათებელი კანის “სამიზნისებრი” გამონაყარით, მაგრამ არანამკურნალები შემთხვევა იწვევს სახსრების, გულისა და ნერვული სისტემის დაზიანებას. სწორედ ამიტომ, ლაიმის დაავადების საწინააღმდეგო ვაქცინის შექმნა დიდი ხანია ინფექციური დაავადებების პროფილაქტიკის ერთ-ერთ პრიორიტეტად რჩება. აშშ-ის დაავადებათა კონტროლისა და ცენტრების (CDC) შეფასებით, მხოლოდ აშშ-ში ყოველწლიურად დაახლოებით 476,000 ადამიანს უდგინდება ლაიმის დაავადების დიაგნოზი ან უტარდება მკურნალობა, ხოლო Pfizer-მა და Valneva-მ თავიანთი უახლესი შედეგების გამოცხადებისას აღნიშნეს, რომ ევროპაში ყოველწლიურად დაახლოებით 129,000 შემთხვევა ფიქსირდება.
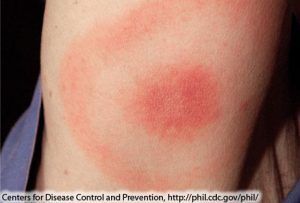
ლაიმისა დაავადების კლასიკური გამონაყარი; წყარო: CDC
ამ ფონზე განსაკუთრებული ყურადღება მიიპყრო Pfizer-ისა და Valneva-ს ერთობლივმა განცხადებამ, რომლის მიხედვითაც მათი კვლევის მე-3 ფაზის (ბოლო ეტაპი დამტკიცების წინ) ვაქცინის კანდიდატმა PF-07307405-მა, რომელიც ადრე VLA15-ის სახელით იყო ცნობილი, ლაიმის დაავადების წინააღმდეგ 70%-ზე მაღალი ეფექტურობა აჩვენა. თუმცა იმავე განცხადებაში იყო ის დეტალიც, რომელმაც ამბავი ბევრად უფრო რთული და საინტერესო გახადა: კვლევამ ფორმალურად ვერ დააკმაყოფილა წინასწარ განსაზღვრული მთავარი სტატისტიკური კრიტერიუმი. ერთი შეხედვით ეს წინააღმდეგობრივად ჟღერს – როგორ შეიძლება ვაქცინა კლინიკურად ეფექტურად გამოიყურებოდეს, მაგრამ კვლევა მაინც ჩაითვალოს წარუმატებლად? სინამდვილეში, ეს არის კლასიკური მაგალითი იმისა, თუ როგორ განსხვავდება ერთმანეთისგან კლინიკური ეფექტი და სტატისტიკური დამაჯერებლობა.
რატომ არის ლაიმის საწინააღმდეგო ვაქცინა ასეთი საყურადრებო მოვლენა
ლაიმის დაავადების საწინააღმდეგო ვაქცინის მიმართ ინტერესი ახალი არ არის. აშშ-ში ადრე უკვე არსებობდა LYMErix – დაავადების საწინააღმდეგო ერთადერთი კომერციულად ხელმისაწვდომი ვაქცინა, რომელიც 1998 წელს გამოვიდა, მაგრამ 2002 წელს მწარმოებელმა ბაზრიდან მოხსნა. CDC პირდაპირ მიუთითებს, რომ ვაქცინა მწარმოებელმა “მომხმარებლის არასაკმარისი მოთხოვნის“ მიზეზით შეწყვიტა, თუმცა ამ ისტორიას თან ახლდა საზოგადოებრივი შიში, უსაფრთხოების ირგვლივ დავები და სასამართლო პროცესებიც, რამაც მთელი სფერო მრავალი წლით შეაფერხა. შედეგად, დღესაც ლაიმის პროფილაქტიკა ძირითადად ტკიპის ნაკბენის პრევენციას, ადრეულ დიაგნოსტიკასა და დროულ ანტიბიოტიკოთერაპიას ეყრდნობა. სწორედ ამიტომ, თუ PF-07307405 საბოლოოდ დამტკიცდება, ეს იქნება პირველი ვაქცინა ადამიანებისთვის 20 წელზე მეტი ხნის შემდეგ.
Pfizer-ისა და Valneva-ს კანდიდატი მეცნიერულადაც საინტერესოა. ეს არის ექვსვალენტიანი OspA-ზე დაფუძნებული ვაქცინა, რომლის სამიზნე ბორელიას გარე ზედაპირულ ცილაა. ამ მიდგომის ერთ-ერთი უნიკალური თავისებურება ისაა, რომ ვაქცინაციის შედეგად გამომუშავებული ანტისხეულები მოქმედებას ფაქტობრივად ტკიპის ორგანიზმშივე იწყებს: როდესაც ტკიპა ვაქცინირებულ ადამიანს უკბენს და სისხლს “წოვს”, ანტისხეულები ხელს უშლის ბაქტერიის გადაცემას ადამიანზე. სწორედ ამ მექანიზმის გამო მიიჩნევა OspA-ზე დაფუძნებული სტრატეგია ლაიმის პრევენციის ერთ-ერთ ყველაზე პერსპექტიულ გზად. ClinicalTrials.gov-ზე განთავსებული ჩანაწერის მიხედვით, VALOR-ის კვლევა შექმნილი იყო იმისათვის, რომ შეეფასებინა ვაქცინის ეფექტურობა, უსაფრთხოება და იმუნოგენურობა ჩრდილოეთ ამერიკასა და ევროპაში, ხუთი წლის და უფროსი ასაკის მონაწილეებში.
რა აჩვენა VALOR-ის კვლევამ
Pfizer-ისა და Valneva-ს მიერ გამოქვეყნებული შედეგების მიხედვით, VALOR-ის მე-3 ფაზის კვლევაში ვაქცინამ 73.2%-იანი ეფექტურობა გამოავლინა, ვაქცინის მეოთხე დოზის მიღებიდან 28 დღის შემდეგ ლაიმის დადასტურებული შემთხვევების შემცირებაში, პლაცებოსთან შედარებით. კომპანიებმა ასევე განაცხადეს, რომ მეორე, წინასწარ განსაზღვრულ ანალიზში ეფექტურობამ 74.8%-ს მიაღწია, და ამავე დროს აღნიშნეს, რომ კვლევის ანალიზის დროს უსაფრთხოების მნიშვნელოვანი სიგნალები არ გამოვლენილა. ეს ნიშნავს, რომ წმინდა კლინიკური კუთხით სურათი საკმაოდ დამაიმედებელი იყო: ვაქცინის ჯგუფში (კვლევის მონაწილეები, რომლებმაც მიიღს ვაქცინა) დაავადების რისკი აშკარად დაბალი აღმოჩნდა, ვიდრე პლაცებოს ჯგუფში (კვლევის მონაწილეები, რომლებსაც ვაქცინა არ მიუღიათ).
აქ ჩნდება სწორედ ბუნებრივი შეკითხვა: თუ ვაქცინის ჯგუფში ნაკლები შემთხვევა იყო და პლაცებოს ჯგუფში მეტი, რატომ ვერ ჩაითვალა კვლევა წარმატებულად? პასუხი ასეთია: დიახ, მიმართულება სწორი იყო – პლაცებოს მხარეს მეტი შემთხვევა უნდა ყოფილიყო და, როგორც ჩანს, ასეც მოხდა – მაგრამ მხოლოდ ეს არ კმარა. სტატისტიკურად საჭიროა, რომ ეს სხვაობა იყოს არა მხოლოდ თვალშისაცემი, არამედ საკმარისად ზუსტად შეფასებული. სხვა სიტყვებით, მკვლევრები უნდა დარწმუნდნენ არა უბრალოდ იმაში, რომ ვაქცინა უკეთესია პლაცებოზე, არამედ იმაშიც, რომ მიღებული სხვაობა შემთხვევითი შედეგი არ არის და მისი რეალური მასშტაბი გარკვეული მინიმალური ზღვარის ზემოთ დგას. სწორედ ამ ეტაპზე აღმოაჩნდა კვლევას სუსტი წერტილი.
მთავარი სტატისტიკური პრობლემა: შემთხვევები ცოტაა, გაურკვევლობა – დიდი
ასეთი მე-3 ფაზის კვლევები ხშირად ე.წ. “მოვლენით ნაკარნახები” ლოგიკით არის დაგეგმილი. ეს ნიშნავს, რომ საბოლოო სტატისტიკური სიმტკიცე ძლიერ არის დამოკიდებული არა მხოლოდ ჩართულ მონაწილეთა მთლიან რაოდენობაზე, არამედ იმაზე, რამდენი “საბოლოო სამიზნე მოვლენა”, ანუ ამ შემთხვევაში რამდენი დადასტურებული ლაიმის შემთხვევა დაგროვდება კვლევის განმავლობაში. შეიძლება კვლევაში ათასობით ადამიანი მონაწილეობდეს, მაგრამ თუ დაავადების შემთხვევები ცოტაა, მაშინ ვაქცინის ეფექტურობის შეფასება ნაკლებად ზუსტი ხდება. Pfizer-მა და Valneva-მ სწორედ ეს განაცხადეს: კვლევის პერიოდში მოსალოდნელზე ნაკლები შემთხვევა დაფიქსირდა, რის გამოც პირველადი ანალიზი საკმარის სტატისტიკურ ძალას ვერ დაეყრდნო. პრობლემა იყო არა ის, რომ ვაქცინამ “არ იმუშავა“, არამედ ის, რომ საკმარისი რაოდენობის შემთხვევა არ დაგროვდა ეფექტის სიზუსტის დასადასტურებლად.
ამ კონტექსტში გადამწყვეტი ხდება სანდოობის ინტერვალი (CI). როცა ამბობენ, რომ ვაქცინის ეფექტურობა 73.2% იყო, ეს არ ნიშნავს, რომ მისი რეალური ეფექტურობა ზუსტად 73.2%-ია. ეს არის საუკეთესო შეფასება მოცემული მონაცემების საფუძველზე. მაგრამ მეცნიერებას სჭირდება მეტი: უნდა იცოდეს, რა დიაპაზონში შეიძლება იმყოფებოდეს რეალური ეფექტურობა. სწორედ ამას აჩვენებს 95%-იანი სანდოობის ინტერვალი. თუ ეს ინტერვალი ფართოა, ეს ნიშნავს, რომ მონაცემებში გაურკვევლობა დიდია; თუ ვიწროა, ეს ნიშნავს, რომ შეფასება უფრო ზუსტია. VALOR-ის შემთხვევაში სწორედ ამ ინტერვალის ქვედა ზღვარი აღმოჩნდა კრიტიკული. პირველ წინასწარ განსაზღვრულ ანალიზში ქვედა ზღვარი იყო 15.8%, მაშინ როცა კვლევის წარმატებისთვის საჭირო იყო, რომ ის 20%-ს გადასცდენოდა. ეს ავტომატურად ნიშნავს, რომ ფორმალური უპირატესი საბოლოო სამიზნე ვერ შესრულდა, მიუხედავად იმისა, რომ ეფექტურობის წერტილოვანი შეფასება მაღალი იყო.
რას ნიშნავს “15.8%-იანი ქვედა ზღვარი“ პრაქტიკულად
ამ დეტალის გასაგებად საჭიროა კიდევ ერთი დაზუსტება. როცა რეგულატორი ან კვლევის წინასწარ განსაზღვრული სტატისტიკური გეგმა მოითხოვს, რომ ეფექტურობის 95%-იანი სანდოობის ინტერვალის ქვედა ზღვარი 20%-ზე მაღალი იყოს, ამით ისინი ამბობენ შემდეგს: “საკმარისი არ არის ვაქცინის საშუალო შეფასება კარგი იყოს; ჩვენ გვინდა დარწმუნებული ვიყოთ, რომ ყველაზე კონსერვატიული, ფრთხილი ინტერპრეტაციითაც კი ვაქცინა მაინც მინიმუმ გარკვეული დონით მუშაობს.“ თუ წერტილოვანი შეფასება 73.2%-ია, მაგრამ ქვედა ზღვარი 15.8%-მდე ეცემა, ეს ნიშნავს, რომ მონაცემები თავსებადია როგორც მაღალი ეფექტურობის სცენართან, ისე შედარებით სუსტი ეფექტის სცენართანაც. ანუ შედეგი იმედისმომცემია, მაგრამ საკმარისად ზუსტი არ არის. სტატისტიკის ენაზე, კვლევამ ვერ “გამორიცხა“ ის ვარიანტი, რომ ნამდვილი ეფექტურობა 20%-ზე ქვემოთ იყოს. სწორედ ამიტომ ჩაითვალა პირველადი ანალიზი ფორმალურად წარუმატებლად.
რატომ შეიძლებოდა შემთხვევების რაოდენობა მოსალოდნელზე ნაკლები ყოფილიყო
ინფექციური დაავადებების კვლევებში ეს იშვიათი არ არის. დაავადების სეზონურობა, გეოგრაფია, ტკიპებთან კონტაქტის რეალური დონე, ამინდი, ეკოლოგიური ცვალებადობა და უბრალო შემთხვევითობაც კი გავლენას ახდენს იმაზე, რამდენი მონაწილე დაინფიცირდება რეალურად. VALOR-ის კვლევაში სწორედ ეს აღმოჩნდა პრობლემური: დაავადების შემთხვევათა რაოდენობა პროგნოზირებულზე დაბალი აღმოჩნდა. ასეთ ვითარებაში კვლევას შეიძლება საკმარისი მონაწილეები ჰყავდეს, სწორი მიმართულების შედეგიც ჰქონდეს, მაგრამ მაინც იყოს არასაკმარისად მძლავრი კონკრეტული წინასწარ გაწერილი კრიტერიუმის შესასრულებლად. ეს არ ნიშნავს იმას, რომ ვაქცინა არაეფექტურია; ეს ნიშნავს, რომ მტკიცებულება ნაკლებად ზუსტი აღმოჩნდა, ვიდრე თავდაპირველად იყო დაგეგმილი.
ეს ისტორია დამატებით რთულ კონტექსტს იძენს იმითაც, რომ 2023 წელს Pfizer-მა და Valneva-მ მესამე ფაზის კვლევის პროგრამაში მნიშვნელოვანი ცვლილებები შეიტანეს და ამერიკაში ჩართული მონაწილეების დიდი ნაწილი კვლევას ჩამოაშორეს, მას შემდეგ, რაც ზოგიერთ კვლევით ცენტრში “კარგი კლინიკური პრაქტიკის” მოთხოვნებთან შესაბამისობის პრობლემები გამოიკვეთა. მოგვიანებით Reuters-მა გაავრცელა ინფორმაცია, რომ აღნიშნულ ცენტრებთან დაკავშირებულ საკითხებზე FDA-მ განზრახ არასწორი ქმედების ნიშნები არ დაადასტურა, თუმცა თავდაპირველმა ჩარევამ პროგრამის მიმდინარეობაზე მაინც მნიშვნელოვანი გავლენა მოახდინა და კვლევის მსვლელობა უკვე ერთხელ შეცვალა. ეს ძველი ეპიზოდი 2026 წლის სტატისტიკურ შედეგს პირდაპირ ვერ ხსნის, მაგრამ ნათლად აჩვენებს, რომ ვაქცინის განვითარების პროცესი თავიდანვე რთული, მრავალფაქტორიანი და ტექნიკური სირთულეებით დატვირთული იყო.
რატომ გახდა მეორე ანალიზი მნიშვნელოვანი
Pfizer-მა და Valneva-მ ყურადღება გაამახვილეს იმაზეც, რომ მეორე, წინასწარ დაგეგმილ ანალიზში სურათი უკეთესი აღმოჩნდა: ეფექტურობა 74.8% იყო და კომპანიების თანახმად, ამ ანალიზშუ უკვე გადაილახა ის სტატისტიკური ზღვარი, რომელიც პირველ ანალიზში ვერ დაკმაყოფილდა. ეს მნიშვნელოვანი დეტალია, რადგან თუ მეორე ანალიზი რეალურად წინასწარ იყო განსაზღვრული სტატისტიკურ გეგმაში, ის ბევრად უფრო ძლიერია, ვიდრე “post hoc”, ანუ შედეგების ნახვის შემდეგ გამოგონილი, “სამაშველო“ ანალიზი. სწორედ ამიტომ აცხადებენ კომპანიები, რომ მიღებული მონაცემები მათ საკმარის თავდაჯერებას აძლევს მარეგულირებლებთან წარსადგენად.
ამ ეტაპზე ყველაზე პრაქტიკული კითხვა ასეთია: რას გააკეთებს FDA და სხვა მარეგულირებლები? საბოლოო პასუხი ჯერ არ არსებობს, მაგრამ არსებული სურათი ასეთია: ერთ მხარეს არის კლინიკურად ძლიერი ეფექტურობა, დამაიმედებელი უსაფრთხოების პროფილი და აშკარა დაუკმაყოფილებელი სამედიცინო საჭიროება, რადგან დღეს ლაიმის დაავადების საწინააღმდეგო დამტკიცებული ადამიანის ვაქცინა არ არსებობს; მეორე მხარეს კი არის ის ფაქტი, რომ პირველადი ანალიზი ფორმალურად ვერ აკმაყოფილებს წინასწარ განსაზღვრულ მთავარ სტატისტიკურ კრიტერიუმს. ამიტომ რეგულატორებისთვის ეს საქმე შეიძლება გახდეს ერთგვარი ტესტი იმისა, რამდენად დიდ წონას მიანიჭებენ ისინი მტკიცებულებათა მთლიანობას და არა მხოლოდ ცალკეულ ბინარულ იარლიყს, დააკმაყოფილა თუ არა კვლევამ კონკრეტული კრიტერიუმი.
რას ნიშნავს ეს პაციენტებისთვის და საზოგადოებრივი ჯანმრთელობისთვის
თუ ვაქცინა დამტკიცდება, ეს იქნება არა მხოლოდ კონკრეტული პრეპარატის წარმატება, არამედ ლაიმის დაავადების წინააღმდეგ პრევენციის სრულად ახალი ეტაპის დაწყება. განსაკუთრებით მნიშვნელოვანია, რომ კვლევაში მონაწილეობდნენ ხუთი წლისა და უფროსი ასაკის პირები, რაც თეორიულად ვაქცინის გამოყენების პოტენციურ მასშტაბს ზრდის. თუმცა დღევანდელი მონაცემებით მთავარი დასკვნა უფრო ფრთხილი უნდა იყოს: Pfizer-ისა და Valneva-ს კანდიდატმა აჩვენა ძლიერი კლინიკური სიგნალი, მაგრამ ამ სიგნალის სტატისტიკური სიზუსტე პირველადი ანალიზის დონეზე ისეთი ძლიერი არ აღმოჩნდა, როგორსაც კვლევის გეგმა მოითხოვდა.
საბოლოოდ, Pfizer-ის Lyme ვაქცინის ამბავი თანამედროვე ბიოსამედიცინო კვლევის ერთ-ერთი ყველაზე კარგი მაგალითია იმისა, რატომ არ არის საკმარისი მხოლოდ ერთი რიცხვის “წაკითხვა”. რეალური კითხვა ყოველთვის უფრო ღრმაა: რამდენად ზუსტია ეს შეფასება, რამდენად ფართოა მისი გაურკვევლობა, და რამდენად მყარად შეუძლია ამ მონაცემს რეგულატორულ, კლინიკურ და საზოგადოებრივ ტესტს გაუძლოს. სწორედ ეს კითხვები განსაზღვრავს ახლა PF-07307405-ის მომავალს.




